Ikatan kimiawi antara molekul oksigen dalam O3 murni kovalen karena atom memiliki nilai elektronegativitas yang identik. Pada ikatan kovalen ini tidak terjadi pengkutuban karena electron tidak ditarik oleh salah satu atom.

Poster Ikatan Kimia Ikatan Kimia Kimia Panduan Belajar
Pengertian Ciri Contoh Soal Senyawa kovalen dibagi menjadi 2 yaitu kovalen polar dan non polar dimana kovalen polar memiliki kutub listrik sedangkan kovalen nonpolar tidak memiliki kutub listrik.
. Ikatan kovalen nonpolar adalah ikatan kovalen yang terbentuk ketika atom membagikan elektronnya secara setara sama. Namun sebagian besar ketika orang berbicara tentang molekul polar mereka berarti molekul kovalen polar dan tidak semua jenis. Ikatan Kovalen Non Polar.
Ikatan antara unsur-unsur ini beragam bergantung pada jenis unsur. Hidrogen sulfida H2S. Ikatan ion membentuk senyawa ion sedangkan ikata kovalen membentuk senyawa kovalen.
Kovalen Polar dan Nonpolar. Molekul senyawa berikut yang bukan merupakan senyawa kovalen polar adalah. Hal tersebut tidak mengakibatkan terjadinya pemisahan kutub oleh karena itu Cl 2 adalah senyawa nonpolar.
Sifat sifat Senyawa Kovalen. H 2 O HI HCl NH 3. Belerang dioksida SO2.
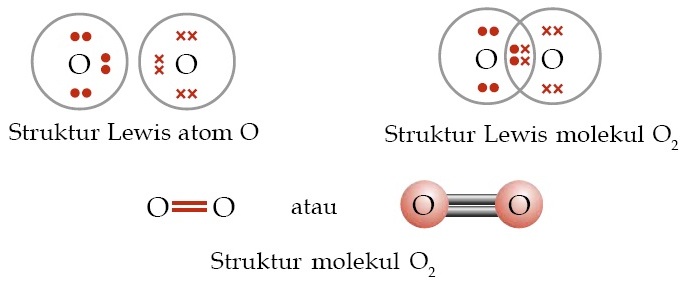
Jika dua atom nonlogam sejenis diatomik membentuk suatu senyawa kovalen misalkan H 2 N 2 Br 2 dan I 2 maka ikatan kovalen yang terbentuk memiliki keelektronegatifan yang sama atau tidak memiliki perbedaan keelektronegatifan. Ikatan yang terjadi antara ion-ion logam dan non logam Ikatan terbentuk akibat gaya tarik listrik antara ion yang berbeda Ikatan ion juga dikenal sebagai ikatan elektrovalen. Pada contoh ikatan kovalen polar yaitu pada molekul HCl pasangan elektron ikatan PEI cenderung tertarik ke salah satu atom yang memiliki elektronegativitas lebih besar yaitu atom Cl oleh karena itu bentuk molekulnya mengutub pada atom Cl sehingga menjadi asimetris tidak simetris.
Memilki titik didih yang relatif tinggi dibawah ikatan ion. Contoh ikatan kovalen non polar. Oleh karena keelektronegatifannya sama besar maka tidak terjadi pengutuban atau polarisasi.
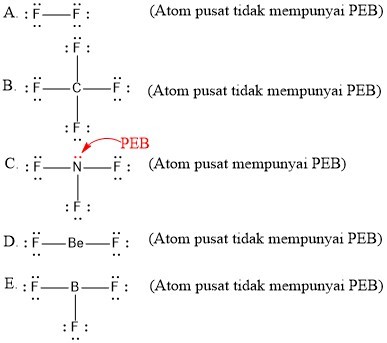
Ikatan kovalen koordinasi hanya dapat terjadi jika salah satu atom mempunyai pasangan elektron bebas PEB. Ikatan kovalen non-polar Dibentuk oleh atom yang identik. Hal tersebut terjadi karena senyawa kovalen polar dalam air akan terdissosiasi menjadi ion-ionnya.
Senyawa kovalen polar dapat menghantarkan arus listrik dalam bentuk lelehannya. Senyawa dapat digolongkan sbagai senyawa ionsenyawa kovalen polar dan senyawa kovalen non polar senyawa manakah yang dapat bersifat elektrolit By admin Posted on Juni 6 2022 Senyawa kovalen polar. Contoh ikatan kovalen nonpolar.
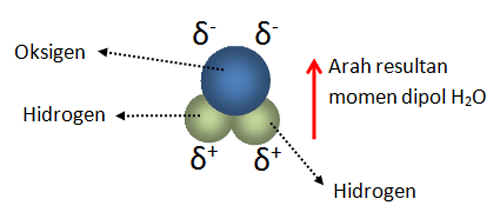
Kepolaran senyawa disebabkan oleh bentuk molekulnya yang simetris atau momen dipol 0. Contoh pada senyawa CH 4. Namun molekul ozon memiliki bentuk bengkok seperti air dan elektronnya tidak menghabiskan waktu yang sama dengan ketiga atom tersebut.
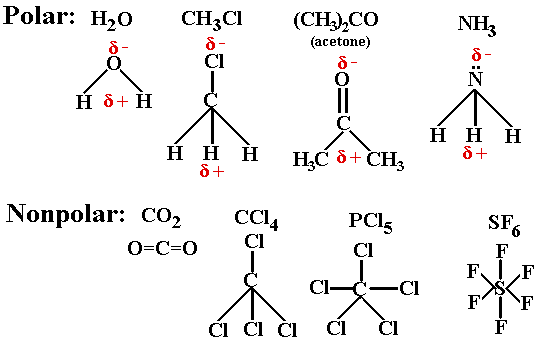
Contoh senyawa lain yang memiliki bentuk molekul simetris dan bersifat nonpolar adalah CH 4 BH 3 BCl 3 PCl 5 dan CO 2. Ikatan kovalen yang terbentuk antara atom dari jenis yang sama biasanya non. Misalnya pada I 2 dimana elektron digunakan oleh dua inti atom I.
Lelehan wujud ini dapat menghantarkan listrik karena dalam bentuk lelehan ion-ionnya bergerak relatif bebas. Molekul Cl 2 terdiri dari 2 atom yang sama yaitu Cl sehingga selisih keelektronegatifannya adalah 0. Perhatikan sifat-sifat senyawa berikut.
Suatu ikatan kovalen bersifat polar apabila distribusi elektron. Senyawa kovalen polar dan nonpolar penyusunnya. Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya.
HCl aq H aq Cl aq H 2 SO 4 aq 2 H aq SO 4 2 aq Beberapa senyawa kovalen polar tidak terdissosiasi sempurna dalam pelarut air sehingga memiliki kemampuan daya. Kepolaran pada molekul ini terjadi karena antara atom H dan atom Cl. Contoh Ikatan Kovalen Nonpolar.
Untuk membedakannya berikut penjelasannya. Secara garis besar ikatan antar unsur dibedakan menjadi dua jenis yaitu ikatan logam dan ikatan kovalen. Biasanya terjadi ketika ada atom mempunyai afinitas elektron yang sama atau hampir sama.
Perhatikan gambar di bawah ini. Contoh senyawa antara lain Air H2O Amoniak NH3 Asam Klorida. Senyawa H 2 merupakan contoh senyawa yang terbentuk melalui ikatan kovalen nonpolar.
Contoh Senyawa kovalen nonpolar diantaranya adalah H 2 O 2 Cl 2 N 2 CH 4 C 6 H 6 BF 3. Senyawa tersebut terbentuk karena unsur-unsur saling berikatan. Semakin dekat nilai afinitas elektron maka semakin kuat ikatannya.
Perhatikan senyawa ionik seperti natrium klorida NaCl bersifat polar. Dalam ikatan kovalen dikenal dengan adanya ikatan kovalen nonpolar dan polar. Ikatan kovalen polar adalah ikatan yang pasangan elektron ikatannya cenderung tertarik ke salah satu atom yang berikatan.
Perhatikan struktur salah satu ikatan kovalen non Polar dari CH 4 berikut. Contoh molekul polar meliputi. Penyataan yang tepat untuk membedakan senyawa ion kovalen polar dan kovalen nonpolar berdasarkan kemampuannya menghantarkan arus listrik adalah.
Yang termasuk senyawa kovalen nonpolar adalah X saja Y saja Z saja X dan Y Y dan Z. Contoh Larutan Elektrolit Senyawa Kovalen Polar. Padatan wujud ini tidak dapat menghantarkan listrik karena dalam bentuk padatan tidak ada ion yang bergerak secara bebas.
Ikatan kovalen tersebut dinamakan ikatan kovalen non polar. Sekarang kami akan bahas sedikit tentang apa perbedaan antara Senyawa dengan ikatan kovalen polar dan non polar. Senyawa kovalen koordinasi adalah ikatan kovalen di mana pasangan elektron yang dipakai bersama hanya disumbangkan oleh satu atom sedangkan atom yang satu lagi tidak menyumbangkan elektron.
Dapat larut dalam air dan pelarut polar lainnya. Senyawa ion dapat menghantarkan arus listrik dalam bentuk padatannya. 14 Agustus 2020 oleh syarief.
Senyawa polar terbentuk dari ikatan kimia dengan nama ikatan kovalen polar sedangkan senyawa nonpolar terbentuk dari ikatan kovalen nonpolar. Ozon adalah contoh molekul polar yang terbuat dari ikatan kovalen nonpolar. Ciri Senyawa Kovalen Polar.
Atom N pada molekul amonia NH3 mempunyai. Hal ini kemudian dinamakan sebagain ikatan kovalen nonpolar. Ikatan antar atomnya bersifat polar namun molekulnya bersifat nonpolar dikarenakan bentuknya yang simetris dengan sudut sama besar.
I 2 Br 2 H 2 N 2. Ikatan Ion Ikatan Kovalen Senyawa Polar Non Polar Gaya antar molekul. Buat kalian yang ingin tau jawaban dari pertanyaan Sifat Senyawa Kovalen Polar Dan Nonpolar kalian bisa simak jawaban yang disediakan dan semoga jawaban dibawah ini bisa membantu kamu menjawab pertanyaan tentang Sifat Senyawa Kovalen Polar.
Nach demikian penjelasan mengenai ikatan kovalen baik yang bersifat polar maupun yang bersifat non polar. Atau Ikatan kovalen nonpolar adalah ikatan kovalen yang Pasangan Elektron. Misalnya Cl 2 O 2 N 2 dll.
Ikatan kovalen polar Terbentuk antara atom yang memiliki perbedaan keelektronegatifan.
10 Contoh Senyawa Polar Dan Nonpolar Materi Kimia

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Catatan Tentang Pas2020 Ikatan Kimia Clear Ikatan Kimia Kimia Panduan Belajar

Ikatan Kovalen Nonpolar Polar Dan Koordinasi Siswapedia

Buat Yang Kelas 10 Yuk Mengenal Ikatan Ikatan Kimia Dalam Atom
10 Contoh Soal Dan Pembahasan Ikatan Kovalen Polar Dan Nonpolar Materi Kimia

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Ikatan Kovalen Polar Dan Nonpolar Penjelasan Perbedaan Dan Contoh

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya
Senyawa Kovalen Polar Dan Nonpolar Materi Kimia

Jelaskan Perbedaan Antara Senyawa Polar Dengan Nonpolar Dan Berikan Masing Masing Contohnya Brainly Co Id

Kimia Kelas X Ikatan Kovalen Polar Non Polar Senyawa Kovalen Polar Dan Senyawa Kovalen Nonpolar Youtube
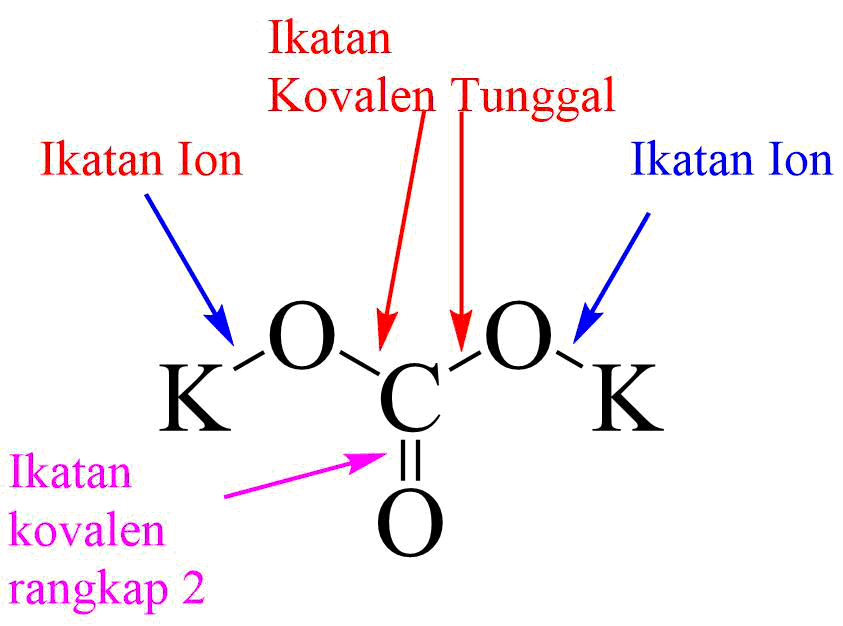
19 Contoh Senyawa Yang Mempunyai Ikatan Ion Dan Kovalen Sekaligus Materi Kimia

Ciri Ciri Ikatan Ion Ikatan Kovalen Polar Dan Nonpolar Brainly Co Id

Ikatan Kimia Pengertian Aturan Jenis Ikatan Kimia Contoh Informasainsedu

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection
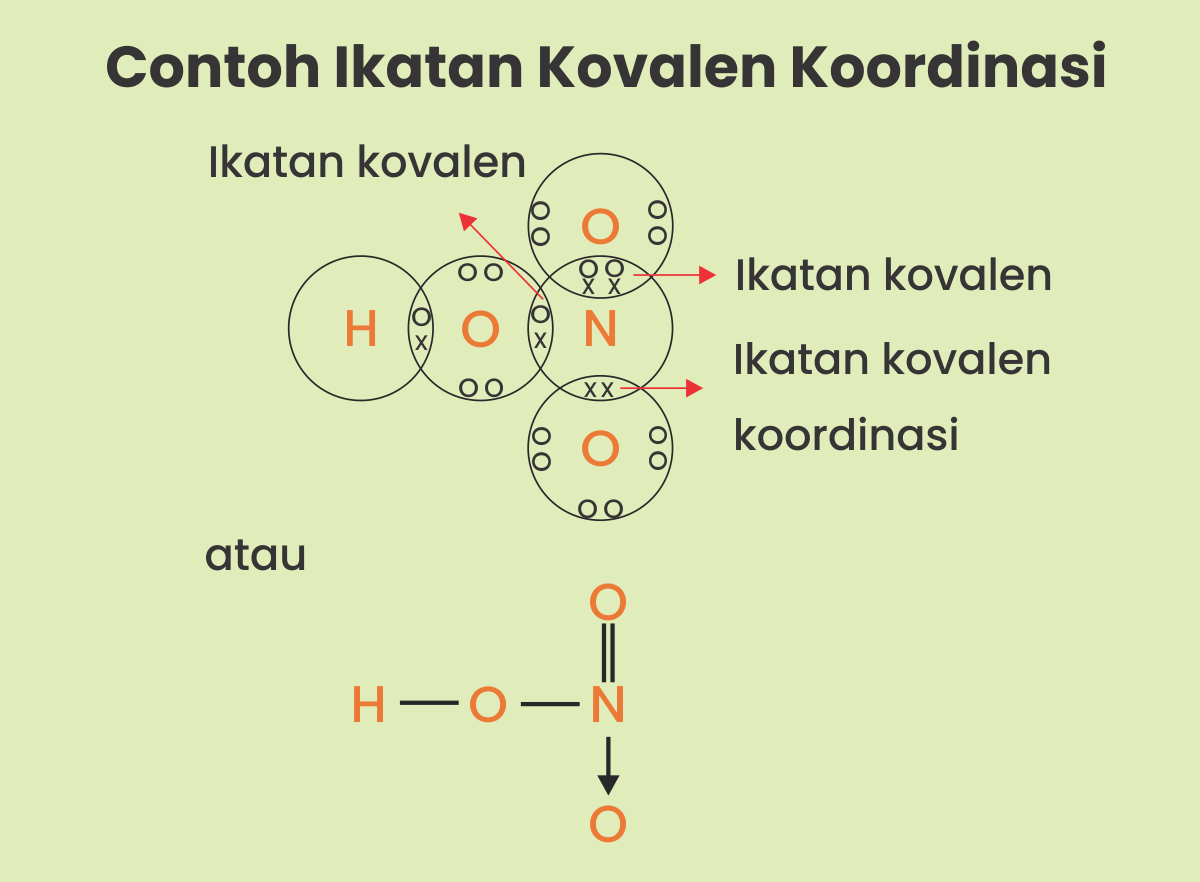
Ikatan Kovalen Nonpolar Polar Dan Koordinasi Siswapedia
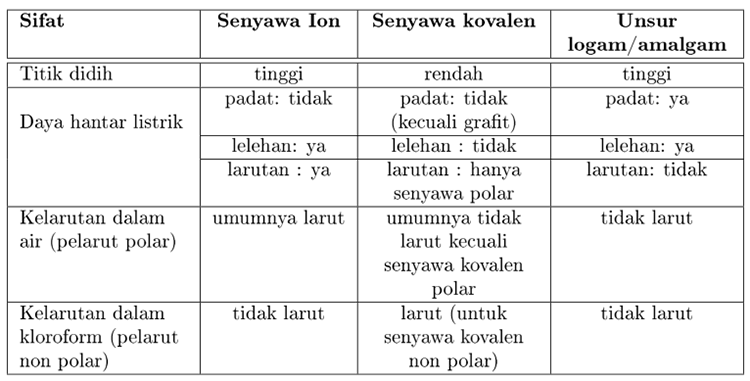
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College

